I temi di ricerca del Traslational Medicine living Lab
I temi di ricerca sviluppati dai partners del Translational Medicine Living Lab includono molte applicazioni di biomateriali avanzati, soprattutto nell’ambito della Medicine Rigenerativa. La neurologia e l’ortopedia rigenerativa sono state il focus principale del progetto Rinovatis, con l’obiettivo di trovare una soluzione alle patologie del Sistema Nervoso Centrale (SNC) e del Sistema Nervoso Periferico (SNP) e di rigenerare i tessuti ossei e cartilaginei affetti da lesioni osteocondrali (OC).
Trattamenti antibatterici a base di argento
La crescente resistenza alle terapie antibiotiche convenzionali e l'attenzione ai costi sanitari hanno di recente incoraggiato lo sviluppo di nuovi approcci nella prevenzione delle infezioni. Le proprietà antimicrobiche dell'argento nei confronti di un ampio spettro di batteri, funghi e virus sono ben note sin dall'antichità e l'argento è oggi usato come agente antimicrobico in un vasto campo di applicazioni. La deposizione di di nano-coatings d'argento su substrati naturali e sintetici può aprire nuovi orizzonti nello sviluppo di biomateriali avanzati intrinsecamente antibatterici.
Nel Dipartimento di Ingegneria dell'Innovazione (DII) dell'Università del Salento, è stata sviluppata una tecnolgia per la deposizione di argento applicata a svariati materiali per le più diverse applicazioni. Il processo, basato sulla sintesi fotochimica e deposizione di coating d'argento in situ, comprende l'impregnazione della superficie con una soluzione a base dìargento e l'irradiazione con luce UV del substrato umido. La perfetta adezione del rivestimento d'argento sul substrato, la capacità antibatteriche e la buona compatibilità a lungo termine sono alcuni dei più importanti risultati ottenuti.
Medicazioni trattate con argento sono stati inoltre progettati per la prevenzione di infezioni associate a ferite difficili, ustioni e ulcere diabetiche; possono essere ottenuti anche materiali tessili smart sia per applicazioni biomedicali che per il confort quotidiano.
Rivestimenti in argento possono essere infine sviluppati per prevenire la formazione di biofilm e infezioni su dispositivi impiantabili come cateteri, protesi e scaffold per la rigenerazione del tessuto osseo e delle ferite.
Scaffold Tessuto Cartilagineo
Scaffold porosi in collagene e chitosano per la rigenerazione del tessuto cartilagineo possono essere ottenuti con la tecnica del freeze‐drying, dal Dipartimento di Ingegneria dell’Innovazione dell’Università del Salento, in collaborazione con Ospedale San Raffaele, CNR-NANO e Università di Bari (Plasmalab). Gli scaffold in collagene mostrano una struttura regolare e omogenea e una porosità isotropa con una dimensione media dei pori pari a circa 0.11 mm sia in direzione longitudinale che trasversale.
La successiva reticolazione del materiale consente inoltre di aumentare significativamente la resistenza meccanica. È possibile inoltre seminare lo scaffold con cellule condrocite fino all’ottenimento di un composito con proprietà simili alla cartilagine, impiegando colla di fibrina per promuovere la sopravvivenza dei condrociti all’interno dello scaffold di collagene 1. La colla di fribrina contribuisce inoltre nel sostenere l’attività sintetica dei condrociti negli scaffold, rendendo questi ultimi biocompatibili e idonei alla rigenerazione del tessuto cartilagineo, dal punto di vista non solo meccanico, ma anche morfologico e chimico.
-
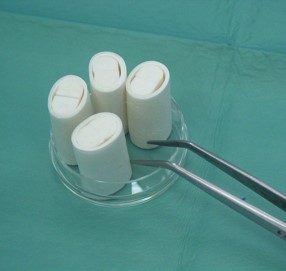
L'immagine raffigura uno scaffold di collagene per la rigenerazione del tessuto cartilagineo.
Scaffold Tessuto Osseo
Tra i diversi materiali ceramici, i fosfati di calcio suscitano un grande interesse come materiali sostitutivi del tessuto osseo, per la loro biocompatibilità e bioattività, caratteristiche che li rendono particolarmente adatti per l’impiego nei settori ortopedico e dentale. Da un punto di vista cristallografico, l’idrossiapatite (HA), è più simile di altri fosfati di calcio alla fase inorganica del tessuto osseo, e quindi rappresenta un miglior materiale strutturale per la crescita ossea.
Sono stati messi a punto, dal Dipartimento di Ingegneria dell’Innovazione dell’Università del Salento in collaborazione con Ospedale San Raffaele e CNR-NANO, innovativi metodi di sintesi dell’idrossiapatite, analizzandone gli effetti sulle caratteristiche morfologiche e chimiche della polvere di HA. Materiali polimerici (collagene) e ceramici (HA) possono essere combinati per ottenere scaffold in grado di rigenerare simultaneamente il tessuto cartilagineo e osso per un trattamento completo del difetto osteocondrale.
-
Sono state messe a punto di tecniche innovative di realizzazione di scaffold 3D con tecnologie al plasma, grazie al supporto dell’Università di Bari (Plasmalab), con HA con struttura porosa e con l’impiego di materiali polimerici che li rendono biocompatibili e idonei alla rigenerazione del tessuto osseo, dal punto di vista meccanico, morfologico e chimico.
Scaffold SNP
I dispositivi sono progettati dal Dipartimento di Ingegneria dell’Innovazione dell’Università del Salento, in collaborazione con Ospedale San Raffaele, CNR-NANO e Università di Bari (Plasmalab), per avere elevate resistenza meccanica e biodurabilità (capacità di resistere alla digestione enzimatica) oltre che per essere biocompatibili. 2 fonti industriali di collagene di tipo I, entrambe ‘FDA approved’ (una isolata da derma bovino e l’altra isolata da tendine equino) sono state caratterizzate dal punto di vista chimico-strutturale, termo-fisico e morfologico mediante, rispettivamente, elettroforesi (SDS-PAGE), spettroscopia infrarossa (FT-IR), alla calorimetria (DSC), termogravimetria (TGA), e alla microscopia (SEM).
La tecnologia di sintesi è basata su una tecnica combinata di spin- casting e freezing e sul processo di freeze-drying, che determina la sublimazione dei cristalli ottenuti con il freezing e produce una struttura altamente porosa. Trattamenti di reticolazione post- fabbricazione consentono di controllare e modulare rigidezza e biodurabilità dei dispositivi, preservandone la biocompatibilità e rendendoli idonei alla rigenerazione del tessuto nervoso, dal punto di vista meccanico, morfologico e chimico.
Possono essere realizzati diversi tipi di scaffold di diverse dimensioni, per gap fino a 30 mm:
-
• Guide neurali tubulari
-
• Matrici con porosità longitudinale
Dispositivi di rilascio
CNR‐NANO, in collaborazione con Dipartimento di Ingegneria dell’Innovazione dell’Università del Salento, Ospedale San Raffaele e Università di Bari (Plasmalab) studiano le strategie migliori d’integrazione delle capsule all'interno di scaffold 3D di diversa tipologia per effettuare il rilascio di fattori per la rigenerazione sia del sistema nervoso periferico che del tessuto ostecondrale.
Sviluppo e ottimizzazione del protocollo di sintesi di capsule di polielettroliti, mediante la tecnica di deposizione strato-su-strato (LbL), hanno consentito la produzione di microcapsule costituite di una cavità e una parete multistrato. Entrambi i compartimenti possono essere funzionalizzati con molecole biologicamente attive. Microsfere a base di acido poli(lattico-co-glicolico) (PLGA) possono essere sintetizzate tramite una tecnica di doppia emulsione “acqua/olio/acqua” (w/o/w) con successiva evaporazione del solvente organico. Tale tecnica è ideale per il loading in PLGA di molecole idrosolubili, quali ad esempio proteine e altri possibili regolatori molecolari, che vengono poi rilasciati gradualmente dalle microsfere nel sito di interesse, sia per diffusione attraverso la matrice polimerica della parete sia per erosione idrolitica della matrice stessa. Il chitosano può essere inoltre impiegato per realizzare microsfere per il rilascio controllato di fattori.
L’integrazione di tali dispositivi negli scaffolds ha lo scopo di:
Aumentare la concentrazione di regolatori molecolari all’interno dello scaffolds mediante immobilizzazione sia all’esterno che all’interno degli scaffolds di un elevato numero di capsule contenenti elevate dosi dei regolatori
Consentire il caricamento di diversi regolatori all’interno dello scaffolds mediante integrazione in esso di capsule contenenti diversi regolatori molecolari
Modulare il rilascio del/i regolatore/i variando la cinetica di degradazione della capsula.
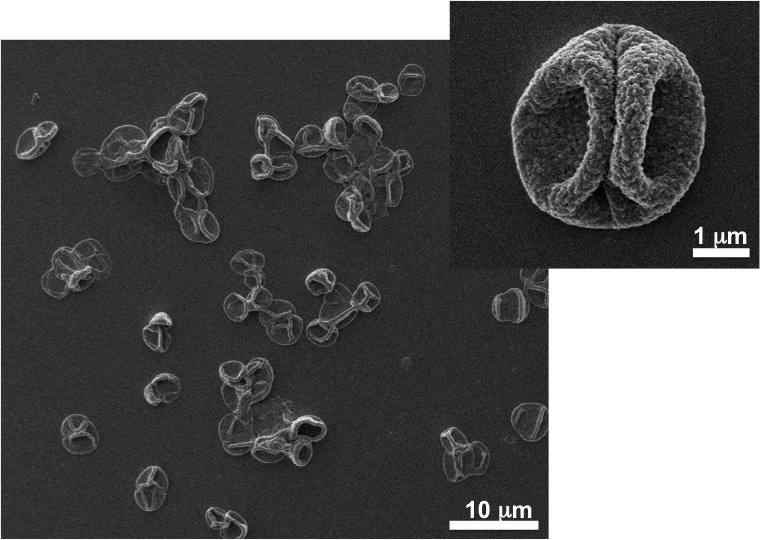
Integrazione di capsule di polielettroliti all’interno dei scaffolds tridimensionali porosi.
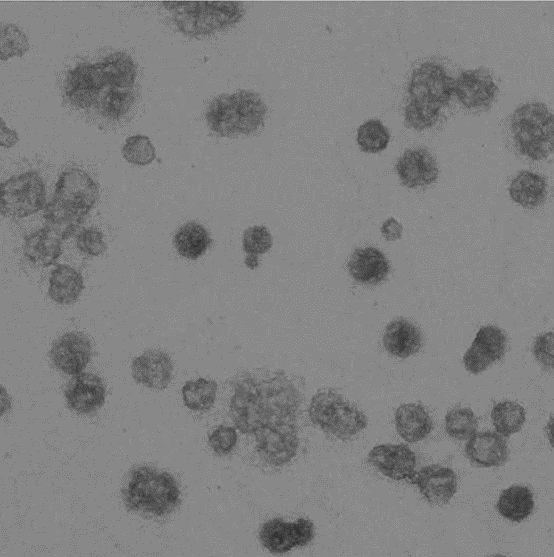
La figura rappresenta un immagine SEM delle microcapsule di polielettroliti.
Funzionalizzazione Scaffold
Processi via plasma, principalmente sviluppati dall’Università di Bari (Plasmalab) possono essere impiegati per l’innesto di gruppi funzionali azotati e ossigenati su matrici di riempimento di guide neuronali. Tali processi hanno come scopo quello di decorare le catene del collagene cross-linkato di gruppi funzionali idrofili (tra cui anche gruppi amminici e carbossilici) al fine di attivare la superficie degli scaffold per la realizzazione di device multifunzionali. Possono essere realizzati:
-
• Processi di immobilizzazione per via umida per l’immobilizzazione di microcapsule su campioni di collagene di tipo I tal quali o modificati via plasma
-
• Processi via plasma a pressione atmosferica direttamente su materiale biologico (cellule e terreno di coltura)
-
L'immagine raffigura la scansione SEM di fibre tessili trattate con nanoclusters di argento antibatterico.
Scaffold SNC
Scaffold microstrutturati possono favorire e guidare la crescita assonale del SNC, così come riscontrato in studi relativi alla rigenerazione del sistema nervoso periferico. Tale scaffold, progettato dai partner Ospedale San Raffaele e Dipartimento di Ingegneria dell’Innovazione dell’Università del Salento, e realizzato in collagene, consiste in un condotto tubolare con porosità radiale, ottenuto mediante la tecnica dello spinning, e due lobi semiellittici, inseriti all’interno del condotto tubolare e aventi porosità orientata in direzione longitudinale o assiale, ottenuti mediante la tecnica del freezing uniassiale. La parte cava del dispositivo ha la funzione di proteggere il sito dell’impianto dall’infiltrazione di tessuto esterno, rimanendo tuttavia permeabile alle cellule dall’interno verso l’esterno; i due lobi interni hanno la funzione di facilitare la ricrescita assonale dei lobi destro e sinistro del midollo spinale lesionato, fornendo agli assoni un adeguato supporto fisico e chemotattico.
-
L'immagine raffigura gli scaffold in collagene per il SNC.
Molecole Bioattive
Mediante analisi di trascrittomica e bioinformatica possono essere condotte indagini, da parte del Ospedale San Raffaele, con il supporto del Dipartimento di Ingegneria dell’Innovazione dell’Università del Salento, sulle molecole in grado di promuovere e guidare la rigenerazione dei tessuti nervosi e osteocartilaginei.
Sebbene laminine, fibronectina, vitronectina e fibrina creano inizialmente un substrato favorevole per i processi rigenerativi, la loro persistenza nel nervo periferico provoca invece un ritardo nei processi rigenerativo, che a lungo andare, causa una progressiva perdita di fibre con insufficiente rigenerazione assonale. Potenziali nuove molecole in grado di promuovere la rigenerazione, in quanto coinvolte nei meccanismi di neurogenesi e morfogenesi d’organo, sono state studiate così come sono stati identificati geni coinvolti nello sviluppo del sistema nervoso. In particolare, i geni TMEM158 e EFBN1 appaiono specificamente espressi dalle cellule di Schwann, che compongono l’assone, e rappresentano quindi geni potenzialmente coinvolti nei processi di mielinizzazione del SNP nella fase di rigenerazione/sviluppo.
-
Nel SNC, la cicatrice astrogliale rappresenta un ostacolo alla crescita del moncone assonale prossimale al danno da taglio o da contusione. BMP signaling attiva la formazione della cicatrice astrogliale, ma è possibile incapsulare gli inibitori di BMP in microsfere di PLGA biodegradabili.
-
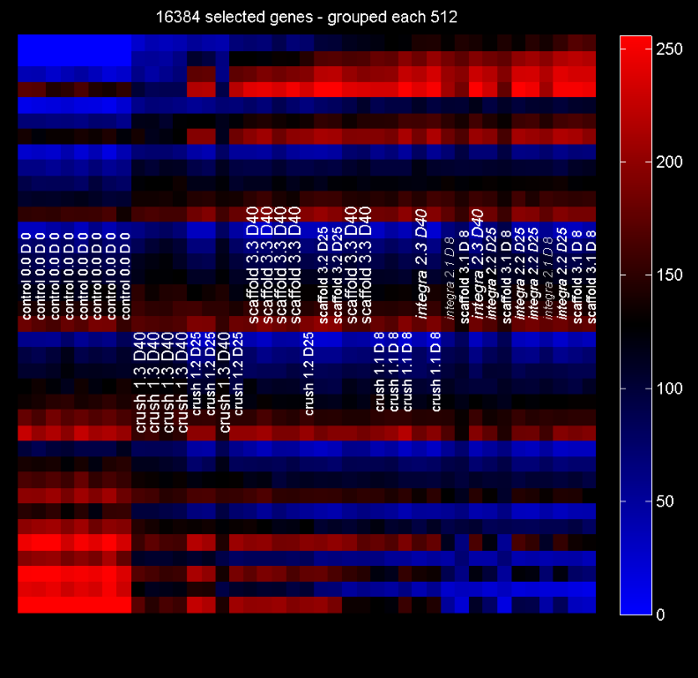
L'immagine rappresenta l'analisi bioinformatica del profilo di espressione del nervo sciatico di ratto.
Analisi di microvescicole
E’ noto che le cellule possono comunicare e scambiare informazioni mediante meccanismi di secrezione, tra questi le vescicole extracellulari: exosomi e microparticelle (MPs) derivate dalla membrana plasmatica. Gli exosomi sono secreti a seguito della fusione di corpi multivescicolari con la membrana plasmatica, mentre le MPs originano direttamente dalla membrana plasmatica. Entrambi gli organelli possono controllare la trasmissione di segnali intercellulari nell’encefalo e svolgere un ruolo nella demielinizzazione immunomediata e nella neurodegenerazione.
Il partner Ospedale San Raffaele riesce a caratterizzare in vitro la natura delle MPs e degli exosomi, utiizzando colture cellulari (cellule mieloidi), stimolate con ATP.
Il partner CNR NANO ha sviluppato un dispositivo nanoPAS (nanoParticle-Analyzer/Sorter), per l’analisi microfluidica, realizzato in PDMS con processi di soft-lithography e che permette la separazione delle nanoparticelle mediante filtraggio idrodinamico. La partnership con la software house Engineering Ingegneria Informatica consente la realizzazione degli algoritmi software per la regolazione della microfluidica del nanoPAS e l’image processing al servizio dell’identificazione e analisi delle microvescicole.
-
L'immagine raffigura un campione di microvescicole.
Biopsia per immagini
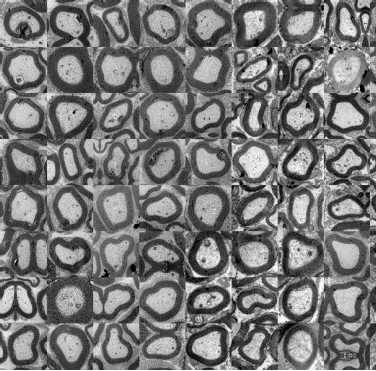
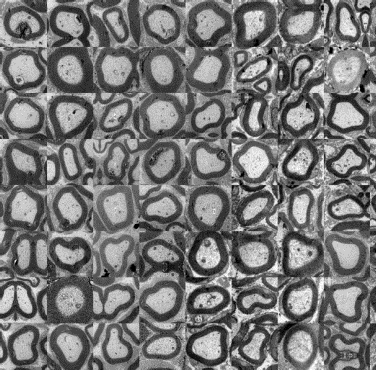
Per valutare l’efficacia dell’impianto in vivo dei dispositivi per la rigenerazione lesioni traumatiche del nervo periferico, Ospedale San Raffaele ha sviluppato nuove metodologie per l’analisi automatica di immagini di sezioni di tessuti nervosi (nervi) ottenute mediante microscopia elettronica, con la collaborazione del DiSTeBA dell’Università del Salento. Le procedure numeriche ed informatiche, necessarie alla registrazione delle immagini acquisite mediante microscopia elettronica, sono state consolidate ed automatizzate al fine di aumentare la produttività mantenendo l'accuratezza dell'analisi comparabile a quella risultante dall'ispezione visiva di personale medico, opportunamente formato e competente.
-
L'immagine rappresenta il montaggio delle fibre nervose selezionate, normalizzate e registrate mediante nuove metodologie di ispezione visiva
sviluppate nel corso del progetto.
Validazione In Vivo
Per quanto attiene alle lesioni traumatiche del SNP e SNC, i modelli murini sono stati considerati i più validi, dato il basso costo, la facilità di mantenimento con possibilità di studio su grandi numeri, le rare infezioni post‐chirurgiche, le validate metodiche di analisi funzionale e istopatologiche. Inoltre, modelli ovini possono essere invece impiegati per lo studio della rigenerazione nervosa di long gap. Combinando tecniche di biologia molecolare, trascrittomica, imaging ad alta risoluzione, microscopia elettronica, transgenesi e neuropatologia, Ospedale San Raffaele, con il supporto del Dipartimento di Ingegneria dell’Innovazione e del DiSTeBa dell’Università del Salento, riesce a stabilire la rilevanza della sintesi proteica assonale in condizioni fisiologiche (crescita assonale, assone adulto normale) e patologiche (danno assonale).
-
Gli animali che sono comunemente utilizzati negli studi di riparazione cartilaginea includono ratti, conigli, cani, capre, cavalli e suini. Animali di piccola taglia sono economicamente convenienti e facili da manipolare, ma limitano il potere di correlare il modello con i risultati attesi nell’uomo. Gli animali di grossa taglia presentano invece uno spessore della cartilagine articolare tale da mimare le lesioni che si osservano nell’uomo, ma sono economicamente svantaggiosi. L'analisi multifattoriale di ciascun modello animale deve essere effettuata al momento di pianificare studi in vivo. Il suino è principalmente usato e il grado di riparazione/rigenerazione può essere valutato ex vivo sia macroscopicamente e biomeccanicamente. Successivamente il tessuto neoformato verrà processato per essere studiato con metodiche microscopiche, biochimiche, immunoistochimiche e di espressione genica.
-
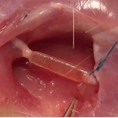
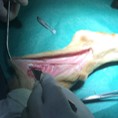
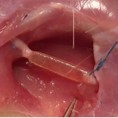
L'immagine rappresenta l'impianto di uno scaffold per SNP su nervo surale di pecora.
Analisi di processo e sperimentazione clinica
In tutte le nazioni facenti parte della Comunità Europea, l’immissione sul mercato, la libera circolazione e l’impiego clinico dei Dispositivi Medici sono regolati dalla Direttiva 93/42/CEE – Dispositivi Medici e successivi aggiornamenti, che definiscono i Requisiti Minimi di Sicurezza a fronte dei quali un determinato prodotto può essere marcato CE e quindi, nel caso di un Dispositivo Medico, utilizzato per l’impiego clinico secondo le Indicazioni d’Uso definite dal fabbricante. Tra i principali requisiti espressi dalla Direttiva c’è l’effettuazione di una Analisi dei Rischi connessi con l’impiego del dispositivo, e la successiva gestione di questi rischi. Le modalità di esecuzione del Processo di Gestione del Rischio, di cui fa parte l’Analisi, sono definite dalla norma tecnica armonizzata EN ISO 14971:2012. Quantificazione e controllo del rischio, valutazione del rapporto rischio/beneficio insieme a quanto altro espressamente richiesto dalla norma, sono attività che il Dhitech Scarl svolge per i dispositivi di tissue engineering sviluppati dai partner e per la loro produzione secondo gli standard di qualità europei. Il Dhitech Scarl ha offerto inoltre il suo supporto per l’analisi della fattibilità di studi clinici per verificare la sicurezza e l’efficacia dei dispositivi nell’uso clinico.